大脑中作用最快的蛋白质之一的新突破性图像提供了关键线索,可能有助于开发治疗癫痫和其他脑部疾病的靶向疗法。该研究结果发表在《自然》杂志上。
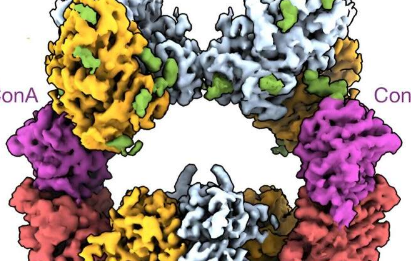
大脑中海人酸受体的闪电般的快速运动对于神经元之间的通讯是必不可少的,但这给试图捕捉受体活动图像的结构生物学家带来了困境。
当被激活时,嵌入在神经元表面的海人酸受体会打开其离子通道,然后在几毫秒内将通道关闭。
“这是结构生物学家面临的关键问题:你必须在通道关闭前瞬间冻结这些分子,”哥伦比亚大学瓦格洛斯内外科医学院生物化学与分子生物物理学副教授亚历山大·索博列夫斯基(AlexanderSobolevsky)说,他领导的团队获得了新图像。
“但冷冻一个分子需要大约30秒,这太慢了。”
这并不是说结构生物学家(获取生命分子图像并建立生命分子模型的科学家)没有尝试过。
海人酸受体功能障碍与癫痫有关,还与抑郁症、焦虑症和自闭症等许多其他脑部疾病有关。它是药物开发商的理想目标,但只有少数获批药物可以安全地靶向该受体。
索博列夫斯基说:“每个人都在尝试获取受体活动的图像,以便我们能够了解其工作原理并设计药物来控制它。”
机器人柱塞减少了冻结分子所需的时间,并有助于捕获处于开放状态的海人酸受体。图片来源:Sobolevsky实验室
两项创新取得成功
Sobolevsky实验室的副研究员ShantiPalGangwar表示:“捕捉活性受体的图像是我们长期以来试图解决的一个科学问题。”通道在激活过程中保持开放的时间只有几毫秒,这个时间太短,无法对受体进行常规冷冻,无法进行低温电子显微镜(cryo-EM)检测,而低温电子显微镜是Sobolevsky实验室用来对生命分子进行成像的结构生物学技术。
为了获得受体活动的图像,Sobolevsky团队开发了两种不同的技术来减缓通道关闭并加速冻结过程。
首先,研究小组寻找能够粘附在受体上并保持其开放的分子。他们发现了两种这样的分子——BPAM和凝集素刀豆球蛋白A。小分子药物样分子BPAM将通道开放时间延长了几百毫秒,但这种延迟仍然不足以捕获处于开放状态的通道。只有在添加凝集素(一种与糖修饰糖蛋白结合的蛋白质)后,通道才能保持开放几秒钟。
电生理记录是确定时间的关键。“通过这些记录,我发现单靠BPAM或凝集素无法维持通道足够长时间的开放,”Sobolevsky实验室副研究员兼电生理学专家MariaYelshanskaya说道。
“当我看到BPAM和凝集素共同产生的协同效应时,我们就像突然灵光一现一样。”
对于传统的低温电子显微镜冷冻技术来说,几秒钟还是太快了,因为传统的低温电子显微镜冷冻技术需要大约30秒才能将样本浸入液态乙烷中并准备好进行成像。因此,Sobolevsky实验室的博士后研究科学家KirillNadezhdin设计了一个机器人柱塞,可以在不到3秒的时间内将样本浸入其中,将受体(与BPAM和凝集素结合)困在开放状态。
利用机器人柱塞和分子稳定器,索博列夫斯基团队捕捉到了多种开放配置下的海人酸受体图像。
“这两项创新都是必要的,”索博列夫斯基说。“我们不可能只用其中一种来捕捉受体的开放状态。”
图像为新药提供线索
开放的海人酸受体的图像为药物开发者提供了关键信息。
有些药物,如离子通道阻断剂,就像葡萄酒瓶塞一样,可以堵塞开放通道。“你需要一个开放通道的结构,才能创造出一种原子间完美契合的药物,”Sobolevsky说。
这些图像还展示了如何优化吡仑帕奈(一种针对海人酸受体的抗癫痫药物),使其能够针对海人酸受体的特定版本,为患者提供更精准的药物。合作者已经在使用Sobolevsky的实验室图像,通过计算机建模探索药物可能的改变。
Sobolevsky团队开发的方法应该可以帮助其他研究人员获得更多开放的海人酸受体和其他类型快速起效分子的图像。
索博列夫斯基说:“我们拥有的图像越多,模型就会越好,希望我们的药物也会越好。”
