根据《自然化学生物学》发表的一项研究,西北医学科学家开发出了一种新的、更精确的方法来针对与某些类型癌症有关的蛋白质。
温伯格文理学院化学助理教授、西北大学罗伯特 H. 卢里综合癌症中心成员张晓宇博士表示,虽然可以通过小分子抑制剂来针对导致癌症生长和治疗耐药性的蛋白质,但这些药物只对一部分蛋白质起作用。
“传统的小分子药物通过直接调节蛋白质活性发挥作用,”张教授说。“挑战在于,一些蛋白质的功能域很难用小分子靶向,例如转录因子、剪接因子等。另一个挑战是蛋白质具有多个功能域,这意味着仅针对其中一个域的小分子可能无法完全抑制蛋白质功能。”
一种有前途的替代方法是使用小分子将蛋白质引导至细胞机制进行蛋白水解降解,从而完全去除蛋白质。
张说:“这种靶向蛋白质降解(TPD)策略可以将无活性的蛋白质结合小分子转化为活性蛋白质降解剂,并具有催化作用,有可能降低达到治疗效果所需的药物浓度。”
越来越多的蛋白质已被证明易受细胞内配体诱导的蛋白质降解的影响。这些结果大多由两种 E3 连接酶介导:CRBN 和 VHL。为了充分发挥 TPD 的治疗潜力,张和他的同事们试图识别其他 E3 连接酶来支持这一策略。
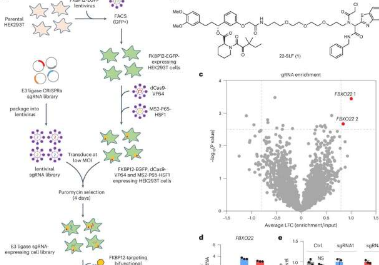
在这项研究中,张和他的同事们利用 CRISPR 筛选发现了能够支持 TPD 的人类 E3 连接酶。研究人员发现,E3连接酶FBXO22 在受到一类名为 PROTAC(蛋白水解靶向嵌合体)的药物刺激后,可以有效介导培养癌细胞内的蛋白质降解。
为了进一步测试他们的方法,研究人员利用他们新开发的化合物来劫持 FBXO22,以降解与白血病和乳腺癌相关的其他几种蛋白质。研究表明,新开发的蛋白质靶向分子能够成功标记蛋白质 BRD4 和 EML4-ALK,以便在癌细胞内降解。
张说,该结果强调了一种针对与人类疾病有关的蛋白质的新方法。
张教授表示:“在许多癌症中,FBXO22 的表达都有所增加。劫持 FBXO22 进行 TPD 可能是一种有前途的方法,既可以靶向癌细胞,又可以降低对正常细胞的毒性。”
在未来的研究中,张教授和他在卢瑞癌症中心的合作者将继续探索 TPD 在不同类型癌症中的应用。
“我们可以用这种方法继续发现能够支持小分子诱导蛋白质降解的新连接酶,”张说。“我们将非常有兴趣进一步探索这些连接酶在不同疾病背景下降解蛋白质的潜力。”
