新方法可使蛋白质药物逐渐释放到体内
近年来,治疗性蛋白质越来越多地用于治疗癌症、艾滋病毒和其他疾病。这类药物的挑战在于释放速度快,因此必须频繁给药。
埃因霍温理工大学(TU/e)物理化学教授RemcoTuinier和他的团队想出了一个解决方案。他们正在开发一种新方法,使蛋白质不再松散地漂浮,而是形成固体包裹。“我预计几年内就能在制药行业看到应用,”Tuinier说。
蛋白质类药物已成为医学界不可或缺的药物。除其他外,它们在新的癌症治疗中发挥着作用。然而,确保这些药物在体内发挥作用是一项挑战。通常剂量给药太快。
蛋白质天生体积小(几纳米),因此扩散速度快。为了确保更慢的释放,更有效的方法是让它们以可控的方式形成更大的颗粒(聚集体)。目前,为此目的使用喷射研磨和喷雾干燥等技术。然而,这些方法可能会破坏蛋白质的化学结构或功能。
工作原理
为了解决这个问题,Tuinier和同事们设计了一种新方法。他们正在与DSMBiomedical合作,后者是一家专注于为生物制药制造商开发材料的全球领先公司。
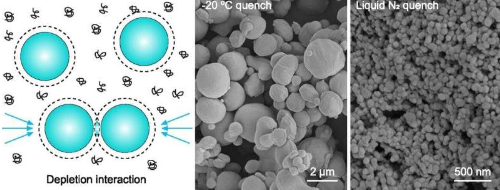
其工作原理如下:首先,将聚乙二醇(PEG)(聚合物)添加到小颗粒混合物中。然后快速冷冻该混合物。PEG有助于将蛋白质适当地浓缩到更大的区域中,然后形成通过冷冻固定的聚集体。
该研究论文发表在《胶体与界面科学杂志》上。
“随着我们添加更多的聚乙二醇,蛋白质变得更粘稠;它们被更紧密地粘在一起。通过将其与冻干相结合,我们可以形成并稳定蛋白质团块。这会导致蛋白质粘在一起形成更大但可控的团块。”
如果这些蛋白质聚集体被“包装”成医疗应用中常用的更大的微米级颗粒,这将有助于更缓慢、更可控地调节药物释放。
Tuinier回忆说,一个重要的里程碑是该论文的博士后兼第一作者宋建康博士发现了第一批微粒。“这是一个激动人心的时刻。当时我们不知道冷冻过程是否会进行得太快,导致蛋白质太小。
“然后我们发现,在冷冻过程中调节最终温度会影响聚集体的大小。然后我们意识到,将快速冷冻与PEG诱导的蛋白质间粘性相结合的基础研究很可能在制药行业中得到有益的应用。”
未来治疗
研究团队现在知道,这种新方法在医学界可能具有巨大价值,因为目前接受癌症治疗的患者通常需要注射药物。由于药物在体内的有效性保持时间更长,因此可以大大减少注射次数。
现在需要优化该方法,Tuinier解释道。“我们正在埃因霍温理工大学与DSMBiomedical合作进一步研究这一问题。为了治疗癌症或HIV,我们需要不同类型的蛋白质,每种蛋白质都具有独特的特性,例如大小和电荷。通过灵活的方法,我们确保我们的方法具有广泛的适用性。”
通常,一种新聚合物需要数年时间才能获得批准,因为需要进行大量测试。“现在情况并非如此,因为我们使用的聚合物已经获得类似应用的批准。”Tuinier预计,几年内,我们将看到使用新方法开发的第一批药物上市。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
截至2024年,大众探岳GTE的售价可能会因地区、配置和促销活动而有所不同。一般来说,2024款探岳GTE的价格可能...浏览全文>>
-
关于2025款途观L的价格信息,目前还没有官方发布。不过,根据以往的市场规律和车型更新周期,我们可以大致推测...浏览全文>>
-
根据您提供的信息,2024款广东东莞威然的最低售价为22 99万元起。关于具体的落地价,需要考虑以下因素:1 ...浏览全文>>
-
根据您的描述,生活家PHEV 2025款的最低售价为 63 98万元起。如果目前有促销活动或优惠政策,建议尽快咨询...浏览全文>>
-
奔腾T99作为一汽奔腾旗下的旗舰SUV车型,凭借其大气的外观设计、丰富的科技配置以及出色的性能表现,吸引了众...浏览全文>>
-
当然可以!以下是一个简单的试驾预约流程,帮助您轻松开启智蓝G5新能源的试驾之旅:1 确定需求- 车型选择...浏览全文>>
-
特斯拉的赛博越野旅行车(Cybertruck)自发布以来就引发了广泛关注。这款车型结合了皮卡的实用性、SUV的多功能...浏览全文>>
-
江淮悍途EV是一款纯电动皮卡,如果您想预约试驾,通常需要满足以下条件和准备以下信息:1 基本条件 - 年...浏览全文>>
-
截至我所掌握的信息,瑞驰新能源的ED75 2024款具体价格和配置可能会因地区、经销商以及政策补贴的不同而有所...浏览全文>>
-
在考虑购买上汽大众ID 4 X时,了解车辆的价格以及相关的购车费用是非常重要的。以下是一些关键信息和费用明...浏览全文>>
- 山东济南途观L新能源价格大公开,买车不花冤枉钱
- 东莞途岳最新价格2025款全分析,买车不踩坑
- 济南探岳GTE新车报价2024款,换代前的购车良机,不容错过
- 郑州ID.7 VIZZION多少钱 2024款落地价,配置升级,值不值得买?
- 郑州途锐新能源最新价格2024款,优惠购车,最低售价67.98万起
- 瑞虎7 PLUS新车报价2025款,买车前的全方位指南
- 广东东莞揽巡价格走势,市场优惠力度持续加大
- 轩逸新车报价2025款,买车前的全方位指南
- 飞凡R7新车报价2025款,换代前的购车良机,不容错过
- 试驾风光ix5,轻松搞定试驾
- 捷途山海L7预约试驾,从预约到试驾的完美旅程
- 试驾E福顺,从预约到试驾的完美旅程
- 长安星卡EV多少钱?选车指南与落地价全解析
- 凯翼E5 EV多少钱?如何挑选性价比高的车
- 标致408X预约试驾,快速操作,轻松体验驾驶乐趣
- 试驾星际牛魔王,新手必看的操作流程
- 岚图汽车岚图梦想家试驾预约,轻松几步,畅享豪华驾乘
- 影豹多少钱?全方位对比助你选车
- 豪运最新价格2023款,豪华配置超值价来袭
- 缤智多少钱 2025款落地价全解买车必看
